我先给大家讲一个真实的故事:故事发生在美国的21世纪初,一个美国高中男孩,很早就知道他的祖父在四十多岁时罹患“亨廷顿氏舞蹈症”,不到50岁就去世了。通过高中生物课,他了解到,“舞蹈症”是常染色体显性遗传病,祖父舞蹈症的致病基因有可能遗传给他,而如果不幸携带了祖父的显性致病基因,他在中年以后必定患病,更加绝望的是,至今,没有任何有效的治疗药物,如同被命运判了缓期死刑。这个男孩决定要去做基因检测,尽早知道自己的命运,如果不幸成为舞蹈症基因的携带者,他要好好享受有限的健康生命,无遗憾的准备迎接发病及死亡的那一天。当然,他更期待抛向空中硬币的另一面的出现:他的细胞内的第四号染色体的DNA序列没有错误。于是,他在家召集同学开了个晚会,隆重地做好第二天接受基因检测的准备。儿子不寻常的举动引起父亲的注意,当得知儿子要去做基因检测的计划后,父亲默默地从枪柜里取出手枪,装上子弹,直奔正在和同学谈笑风生的儿子,用枪抵住男孩的脑袋,大声呵斥:如果你敢去做那个基因检测,我就打碎你的脑袋。周围的同学们被吓呆了,面面相觑,纷纷告辞离开。直到男孩承诺永远取消基因检测的计划,父亲的手枪才缓缓的放下。父亲喘着粗气,瘫坐在沙发上。
从遗传学的视角看,祖父携带常染色体显性致病基因,其子女有50%概率被遗传,这位父亲非常明白,他在忐忑和不安中度过了40年,如果同样不幸携带舞蹈症致病基因,其距离发病的大限越来越近了,但他不想知道确切的未来,宁愿把人生交给命运,赌那幸运的50%概率。然而,儿子的决定将打破未知结果的赌局,如果儿子是致病基因的携带者,作为父亲的他必然是舞蹈症的未来病人,而且,发病期限临近,这个父亲无法接受这个被揭示的确切人生定数,于是,发生了刚刚的一幕,他用手枪对准了儿子的脑袋:宁可犯罪,杀死自己亲生骨肉,也不想明确自己的注定命运。
以上这个故事涉及到一个单基因的显性遗传病,遗传学、病原学、病理生理学、临床表现均已比较明确,按常规的科学思维,既然现代基因检测技术可以100%明确诊断,实现早期诊断,即使没有有效治疗手段,让携带者可以好好规划自己的有限生命,应该是好事,但是,作为风险人群的个体,他们的顾虑、挣扎和对命运的无奈是痛苦的,对基因检测预知未来的取舍是矛盾的。同时,社会的可能歧视也会造成不可估量的后果。美国曾经在70年代实施过“镰刀性贫血”的基因普查,因绝大部分致病基因携带者为黑人,当结果公布后,黑人儿童经历了失学、被医疗保险拒绝等歧视行为。
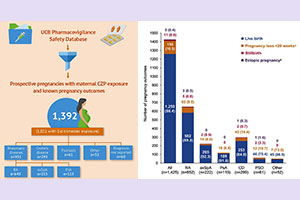
今天,第四代基因检测技术已经诞生,将全基因测序的的时间缩短到几个小时,费用降低到百元美金,成为了人人可以负担的起的常规临床检测。同时,将疾病的诊断、预后、治疗及转归作为观察指标,实施与基因信息相关性的队列研究大量开展,形成了基于多基因的疾病风险评分(polygenic risk score, PRS)的预测模型,辅助临床决策。
多基因风险评分综合了人类基因组中等位基因的许多小效应(small effects),以评估个体疾病或疾病相关特征的风险。PRS的潜在益处包括提高原发病预防的成本效益、更精确的诊断以及提高药物处方的准确性。然而,必须将这些因素与潜在风险进行权衡,例如PRS表现的不确定性和偏倚,以及在医疗实践中对这些因素可能存在的误解和误用;同时,更依赖后天生活习惯及环境的表观基因,对健康与疾病也起到重要作用,而目前的PRS并未涉及。当然,本文故事中展现的医学伦理、个人的偏好和社会偏见的可能风险也应被充分考虑。通过解决关键问题,包括弥补最佳做法、风险沟通和监管框架方面的差距,PRS可以负责任地用于改善人类健康。在此,国际常见病联盟的PRS工作组(一个由遗传学、法律、伦理学、行为科学等领域的专家组成的多学科小组)重点介绍了最近的研究,以全面总结多基因评分研究的现状,以及PRS在临床上广泛应用的需求和挑战。
请关注:在临床上负责任地使用多基因风险评分的益处和风险。