一般来说,只要疫苗接种率及感染率能达一个阈值,传染病即可被控制,停止传播,此状态被称之为群体免疫,而群体免疫将使社会恢复正常。新冠病毒的群体免疫阈值定为60%-70%的人群获得免疫力。但随着COVID-19大流行进入第二年,科学家们的想法开始转变。其中,两个残酷的事件击垮了实现群体免疫的常规思维。
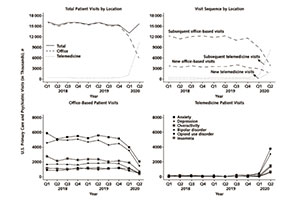
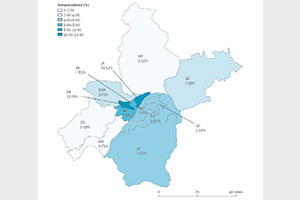
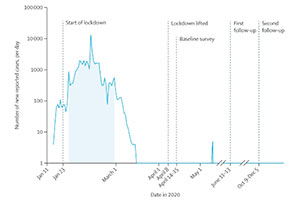
巴西发生的事件让理想不再丰满。发表在《科学》(Science)杂志上的研究表明,2020年5月至10月间,巴西马瑙斯市COVID-19的下降可能归因于群体免疫效应。巴西圣保罗大学的免疫学家Ester Sabino和她的同事计算出,到2020年6月,该地区已经有超过60%的人口被感染。根据一些估计,这本应足以使人群达到群体免疫阈值,但在2021年1月份,马瑙斯市的感染病例大幅回升。这一高峰发生在一种被称为P.1的新变种出现之后,这表明以前的感染并不能给病毒提供广泛的保护。Sabino说:“1月份,马瑙斯市的病例100%是由P.1引起的。”美国波士顿东北大学的Scarpino怀疑原来60%的感染率数据可能被高估了。
印度发生的事件让现实更加骨感。自2021年3月,印度迎来了第二波疫情。世卫组织首席科学家苏米娅·斯瓦米纳坦日前在接受媒体采访时指出,因为印度国内核酸检测能力有限,印度疫情局势或被严重低估,印度实际感染人数有可能是现公布人数的20到30倍。如果按照该名科学家的说法,印度现如今新冠肺炎感染人数有可能已经达到了3.5亿至5.3亿左右。这个接近50%感染率的群体免疫率,加上接近10%的疫苗接种率,并没有阻止病毒的传播和疫情的蔓延。在新冠病毒大流行的历程中,群体免疫的概念成为空无的兴奋剂和放松警惕的麻醉剂。
包括顶级的流行病学专家,已将其COVID-19预测模型的名称从“群体免疫路径”修改为“回归正常路径”。
为什么现实很骨感?目前可陈述的科学理由有以下几点:
1、目前不清楚疫苗是否能阻断传播:包括最有效的mRNA疫苗,仅仅有预防新冠病毒感染发病的证据;
2、疫苗推广不均衡:在发达国家,高比例的人群拒绝接种疫苗,儿童接种率极低,形成了易感人群,在发展中国家,疫苗的可及性十分令人担忧;
3、新变种改变了群体免疫:疫苗接种的不充分性,以及疫苗本身给病毒造成的进化压力,都让病毒变异成为不可避免的现实;
4、免疫力可能不会长久:已经有多起罹患新冠病毒病后及接种疫苗后再感染同种病毒的研究报道;
5、疫苗可能会改变人类行为:人们误以为疫苗是“防弹衣”,彻底忘记了保持社交距离及佩戴口罩的经典防护措施,不仅仅是让易感人群处于危险地位,也让疫苗保护无效的人群成为高危感染者。
因此,新冠病毒很可能会成为一种新的非季节性“流行性病毒综合征”,人类要抛开群体免疫的幻想,更不要奢望像对付SARS一样将它们清除,要做好与新冠病毒共生存的准备,而且是全天候的伴随。针对那些不断变异,躲避我们免疫力的变异病毒,必须依赖科学的手段:发现、测序、快速发明疫苗、产业化、平等的分配和接种。值得让人们兴奋的事实,应该包括“疫情带来的副作用”:流感的发生率在过去的一年创造了历史最低纪录。而这一不意外的奇迹首先要归功于人们主动或被动的采取了经典的手段:保持社交距离及佩戴口罩。依靠科学,回归经典,是让丰满的理想成为美好现实的必由之路。
请关注本期COVID-19专题:COVID群体免疫,为什么是不可能的?