每当一种新的疾病出现,科学家们会从两个途径寻找治疗方法:一个就是针对新的病原、病因开发新的治疗手段;另一个则是根据病理生理,寻找与已知疾病共同的规律,从老药或在研新药中筛选出治疗新病的武器。前者未知数大、失败风险高、耗时长;后者把握大、成功几率高、发展迅速。前者早期依赖基础研究的科学家,医药企业主导,临床医生按药物研发阶段介入,如同田径场上的接力赛;后者以临床医生为主导,借力基础研究成果和临床体会,快速实施临床老药新用验证,如同战场上的冲锋。前者人体中的疗效及安全性不得而知;后者至少在安全性上已经过一定人群及时间的检验。但是,前者容易一鸣惊人,得到政府及企业的青睐支持,商业利益大;后者常常显得平常、理所当然,不受政府重视、企业不感兴趣,商业利益小。
历史上,这样的例子数不胜数,第一代的肿瘤化疗药,如:甲氨蝶呤、硫唑嘌呤,均在临床医生的创意下,成为治疗类风湿关节炎、系统性红斑狼疮的一线用药;抗艾滋病病毒的药物,如:拉米夫定,在临床医生的尝试下,成为第一个可以治疗乙型病毒性肝炎的药物;西地那非治疗心衰的临床试验虽然失败,但其副作用成就了第一个治疗勃起功能障碍的万艾可。
当新冠病毒病(COVID-19)突袭武汉之际,治疗埃博拉病毒的试验药物瑞德西韦迅速调转防线,瞄准了新冠病毒(SARS-CoV-2),开展了临床研究。COVID-19和埃博拉病毒虽然不是一个家族,但都属于RNA病毒,都需要RNA依赖型RNA聚合酶(RdRp)的参与,而瑞德西韦正是RdRp的抑制剂,从机理上讲,瑞德西韦可以抑制SARS、MERS、埃博拉和新冠病毒,且得到了体外研究证实。尽管瑞德西韦的临床研究并不经典,无清除病毒的终点,美国FDA还是基于临床急需治疗药物、新药及疫苗的研发还需时日,特别批准了瑞德西韦的临床应用。
无独有偶,从机制及体外研究层面,爱若华(来氟米特)能有效干扰病毒包膜或核壳体的合成及组装,抑制病毒基因的复制和早期病毒基因的表达以及宿主细胞的增殖,影响细胞内信号传导通路。2003年,我国国家药物筛选中心抗SARS病毒筛选中心研究发现:来氟米特的活性代谢产物(A77 1726)对SARS病毒具有抑制作用,能保护被感染的细胞;2020年3月,武汉大学病毒学国家重点实验室和华东理工大学药学院/上海市新药设计重点实验室合作的研究,报道了针对DHODH作为靶点,筛选抗新冠病毒肺炎候选药物和老药品种。研究的药物中,已有的作为DHODH抑制剂的老药就是来氟米特和特立氟胺,结果显示该系列抑制剂对多种RNA病毒都具有广谱抗病毒活性,通过抑制嘧啶合成,也可抑制SARS、MERS、埃博拉和新冠病毒。来氟米特的活性代谢产物特立氟胺,在细胞水平抗SARS-CoV-2的EC50为6μM~26μM,而该水平在治疗类风湿关节炎有效剂量的血药浓度范围内,提示老药来氟米特或特立氟胺可能具有较好的抗新冠病毒的临床应用潜力。
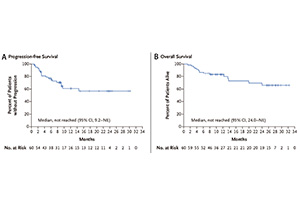
从临床研究层面,来氟米特能有效治疗BK多瘤病毒、巨细胞病毒及人乳头瘤病毒等感染。2020年3月~4月,山东大学齐鲁医院胡昭教授组织单中心、开放标签、对照研究(非随机),比较常规治疗(羟氯喹+阿比朵尔)与来氟米特联合治疗(常规治疗+来氟米特)对新冠病毒PCR持续阳性、长病程的COVID-19患者的抗病毒有效性及安全性,研究主要针对病程在28天以上的难治性患者。结果显示:14天病毒转阴率80.0% vs 16.7% (来氟米特 vs 常规治疗组, P=0.002);14天出院率73.3% vs 8.3% (来氟米特 vs 常规治疗组,P=0.001)。因此与常规治疗相比,来氟米特(20mg/d~30mg/d)联合治疗长病程、难治性COVID-19患者,显著升高病毒转阴率和患者出院率,缩短患者转阴及出院时间,该研究成果2020年6月发布在医学预印本网站medRxiv上。2020年5月,美国芝加哥大学注册了来氟米特治疗COVID-19的临床研究(NCT04361214),目前正在开展中。7月,武汉大学人民医院的一项小规模临床研究发表在《Virologica Sinica》杂志,研究显示来氟米特能有效加快病毒转阴,较对照组减少6天。
面对新冠病毒的全球大流行,WHO极力推动老药新用的临床研究及应用,但至今仍没有奇迹出现。或许,爱若华可能为控制新冠病毒带来一线希望的曙光。古有“一箭射双雕”,今有“一药治多病”,爱若华的科学实践,续写着“异病同治,同病异治”的中国智慧。
请关注本期COVID-19专题:“抗击新冠病毒的中国智慧”以及“寻找治疗COVID-19 的药物——从WHO 到中国”。